№ п/п | Название работы | Оборудование и реактивы |
1 | Приемы обращения с лабораторным оборудованием | Оборудование: Штатив, спиртовка, лабораторная посуда. |
2 | Очистка загрязненной поваренной соли | Оборудование: смесь песка с солью, 2 стаканчика, стеклянная палочка, промывалка с водой, фильтр, воронка, спички, спиртовка, зажим, чашка для выпаривания. |
2 | Анализ почвы и воды | Оборудование: две пробирки, воронка, бумажный фильтр, стеклянная палочка, предметное стекло, спиртовка, стеклянный цилиндр с водой, пробка, универсальная индикаторная бумага. |
3 | Наблюдение за горящей свечой | Оборудование: Свеча, резиновая груша, пробирки, предметное стекло, 2 химических стакана разного размера. Реактивы: Известковая вода. |
4 | Приготовление растворов | Оборудование: Мерный цилиндр, коническая колба, лабораторные весы. Реактивы: Сахар, вода. |
5 | Признаки химических реакций | Оборудование: спиртовка, штатив с пробирками. Реактивы: медная проволока, H2SO4, HCl, роданид калия (KSCN), мел (CaCO3), FeCl3, Na2СO3, СaCl2. |
6 | Ионные реакции и условия их протекания | Оборудование и реактивы: пробирки, растворы сульфата меди (II), гидроксида натрия, хлорида бария, карбоната натрия, азотной кислоты, серной и соляной кислот, фенолфталеин. |
7 | Свойства кислот, оснований, оксидов и солей | Оборудование: штатив с пробирками. Реактивы: HCl, NaOH, Na2CO3, AgNO3, BaCl2, H2SO4, FeCl3, фенолфталеин. |
8 | Решение экспериментальных задач | Оборудование: спиртовка, штатив с пробирками. Реактивы: KCl, MgSO4, Zn, PbNO3, BaCl2, H2SO4 |
Практическая работа № 4.
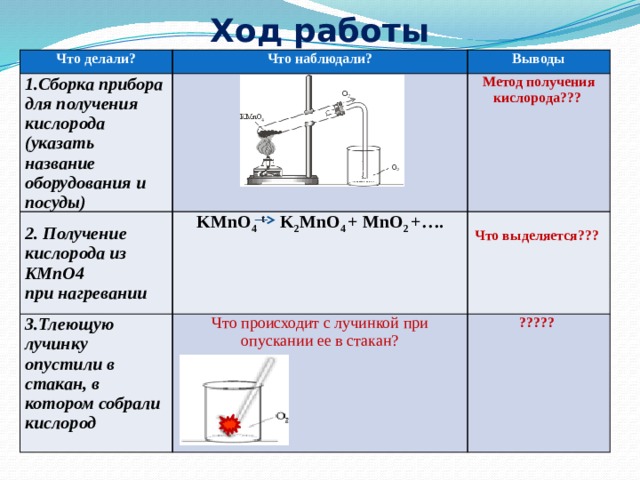 Признаки химических реакций
Признаки химических реакцийПрактическая работа включает четыре опыта.
Опыт 1
Прокаливание медной проволоки и взаимодействие оксида меди (II) с серной кислотой
Зажгите спиртовку (газовую горелку). Возьмите тигельными щипцами медную проволоку и внесите ее в пламя. Через некоторое время выньте проволоку из пламени и счистите с нее образовавшийся черный налет на лист бумаги. Опыт повторите несколько раз. Поместите полученный черный налет в пробирку и прилейте в нее раствор серной кислоты. Подогрейте смесь. Что наблюдаете?
Образовалось ли новое вещество при накаливании меди? Запишите уравнение химической реакции и определите ее тип по признаку числа и состава исходных
веществ и продуктов реакции. Какие признаки химической реакции вы наблюдали? Образовалось ли новое вещество при взаимодействии оксида меди (II) с серной кислотой? Определите тип реакции по признаку числа и состава исходных веществ и продуктов реакции и запишите ее уравнение.
1. При прокаливании медной проволоки медь окислятся:
и образуется черный оксид меди (II). Это реакция соединения.
Это реакция соединения.
2. Образовавшийся оксид меди (II) растворяется в серной кислоте, раствор становится голубого цвета, образуется сульфат меди (II):
Это реакция обмена.
Опыт 2
Взаимодействие мрамора с кислотой
Положите в небольшой стакан 1—2 кусочка мрамора. Прилейте в стакан столько соляной кислоты, чтобы ею покрылись кусочки. Зажгите лучинку и внесите ее в стакан.
Образовались ли новые вещества при взаимодействии мрамора с кислотой? Какие признаки химических реакций вы наблюдали? Запишите уравнение химической реакции и укажите ее тип по признаку числа и состава исходных веществ и продуктов реакции.
1. Мрамор растворился в соляной кислоте, произошла химическая реакция:
Опыт 3
Взаимодействие хлорида железа (III) с роданидом калия
В пробирку налейте 2 мл раствора хлорида железа (III), а затем несколько капель раствора роданида калия KSCN — соли кислоты HSCN, с кислотным остатком SCN—.
Какими признаками сопровождается эта реакция? Запишите ее уравнение и тип реакции по признаку числа и состава исходных веществ и продуктов реакции.
Раствор стал ярко-красным, образовался роданид железа (III):
Это реакция обмена.
Опыт 4
Взаимодействие карбоната натрия с хлоридом кальция
В пробирку налейте 2 мл раствора карбоната натрия. Затем добавьте несколько капель раствора хлорида кальция. Что наблюдаете? Запишите уравнение химической реакции и укажите ее тип по признаку числа и состава исходных веществ и продуктов реакции.
Наблюдается выделение белого кристаллического осадка сульфата бария:
Это реакция обмена.
Источник:
Решебник
по
химии
за 8 класс (О.С.Габриелян, 2011 год),
задача №4
к главе «Глава 5. Простейшие операции с веществами (химический практикум). ».
Все задачи
← Практическая работа № 3. Анализ почвы и воды
Практическая работа № 5. Приготовление раствора сахара и расчет его массовой доли в растворе →
8 -й класс Физическая наука — Обучение неограниченному департаменту науки о подготовительной школе
Science 2022-2023
класс 8
Учитель: г -жа Preeti Notani
I. Учебная программа
Учебная программа
класс 8
Курс. Научный класс 8-го класса изучает материю, энергию и их взаимосвязь. Этот курс охватывает основы химии и физики. Студенты будут проводить время, работая в лабораторных условиях, чтобы применять изученные принципы, улучшать лабораторные методы и больше узнавать об окружающем мире. Умение применять полученные знания в повседневной жизни является главной целью этого класса.
Основные области обучения будут включать: обучение использованию различных типов измерений, сила, работа, движущиеся объекты, классификация материи, периодическая таблица, закономерности в различных элементах, химические реакции, основы органической химии, простые и сложные машины, волны, свет, звук, тепловая энергия, электричество и магнетизм.
Мы охватим большую часть информации в тексте, но я буду использовать другие дополнительные материалы. Особое внимание уделяется решению научных задач и навыкам мышления более высокого уровня. Занятия в классе: лабораторные занятия, виртуальные лаборатории, видеоролики, демонстрации, лекции в Power Point и лабораторные отчеты.
Занятия в классе: лабораторные занятия, виртуальные лаборатории, видеоролики, демонстрации, лекции в Power Point и лабораторные отчеты.
Неделя 1 (с 18 по август — 19)
Обработки конверсии
Безопасность
Лабораторное оборудование
Неделя 2 (22 августа — 26)
Ch 1: Движение
Словарь
Глава 1.pptx
Файл загрузки.
Неделя 3 (29 августа — 2 сентября)
Тема: Скорость и ускорение
Практика
POWER POINT
Неделя 4 (5 сентября — 9 ) 5
Глава 2: Законы движения 12 сентября — 16)
Глава 2 Обзор
Неделя 6 (неделя с 19 по 23 сентября)
Основная тема
Глава 3 Работа и простые машины и инженерные проекты
Словарь
Пт. Подготовка
Презентация проектов STEM
Неделя 8 (3 октября — 7 октября)
No School
Неделя 9 (11 октября — 14 октября)
Ch 3
. 17 окт — 23)
Глава 4: Силы и жидкости
Неделя 11 (24 октября — 28 октября)
Обзор понедельника, главы 4
Словарь
Неделя 12 (31 октября — 4 ноября)
Глава 5 Ted Talk and Thermal Energy Проекты
Неделя 13 (7 ноября — 11 ноября)
Energy Ted Talk
Неделя 14 ноября 2022 г.
CH 5 и 6 Словарь с примерами
Неделя 14 (14 ноября — 18)
5 и 6
Неделя 15 (21 ноября — 23 ноября)
Мон-викторина по главам 5 и 6 (лаборатория — мощность вертушки)
Понедельник-глава 7: Основы химии
Словарь
Неделя 16 (28 ноября — 2 декабря)
Понедельник-глава 7 — Повторные вопросы
Midterms- Ch 1-7
Неделя 3-го января
Science Fair-CH 8: штаты Материя
Словарь
неделя 9 января
CHMAPTE Научная ярмарка
Неделя с 16 января
Глава 9 Атомные теории и научная выставка
Неделя с 23 января
Глава 10 Периодическая таблица, лекция и заметки
Неделя с 30 января по 9 февраля, 9 февраля и научная ярмарка
Глава 11 Химические связи и
Неделя от 13 февраля
Отчет научной ярмарки и эксперимент будут оцениваться
Неделя от 27 февраля
Химическая ярмарка 2023
9 марта 0
Неделя
0010
Неделя 13 марта
Глава 12 Обзор и испытание
Неделя 20 марта
Обзор Урок 1: Вещества и смеси Лекция и лабораторная работа
Урок 2: Свойства растворов / лекция 3 и лабораторная работа 90 Учебное пособие по основным растворам
Неделя с 27 марта
Глава 13 Обзор формул соединений, кислот и оснований (проверьте электронную почту для получения задания) W
Неделя с 3 апреля — Глава 14 Органическая химия
0010
Обзор главы Урок 1: Элементарный углерод и простые органические соединения
Урок 2: Другие органические соединения
Урок 3: Соединения жизни Учебное пособие
ГЛАВА 1 ОПИСАНИЕ ДВИЖЕНИЯ
ГЛАВА 2 ЗАКОНЫ ДВИЖЕНИЯ
ГЛАВА 3 РАБОТА И ПРОСТЫЕ МАШИНЫ
ПРОСТЫЕ МАШИНЫ ПРОЕКТГЛАВА 4 СИЛЫ И ЖИДКОСТИ
ОЦЕНКА ЖИДКОСТЕЙ CH 4
ГЛАВА 5 ЭНЕРГЕТИКА И ЭНЕРГЕТИЧЕСКИЕ РЕСУРСЫ
ч 5 викторина
Ч. 5 ТЕСТ
5 ТЕСТ
ГЛАВА 6 ТЕПЛОВАЯ ЭНЕРГИЯ
ГЛАВА 6 ВИКТОРИНА
ГЛАВА 7 ОСНОВЫ ХИМИИ
ГЛАВА 7 ВИКТОРИНА
ч. 7 ОСНОВАНИЕ CHEM MC
ГЛАВА 8 СОСТОЯНИЯ ВЕЩЕСТВА
ГЛАВА 9. ПОНИМАНИЕ АТОМА
ГЛАВА 10 ПЕРИОДИЧЕСКАЯ ТАБЛИЦА
ч. 10 стр.
CH 11 ЭЛЕМЕНТЫ И ХИМИЧЕСКИЕ СВЯЗИ
ГЛАВА 12 ХИМИЧЕСКИЕ РЕАКЦИИ И УРАВНЕНИЯ
CH 13 СМЕСИ, РАСТВОРИМОСТЬ И РАСТВОРЫ КИСЛОТЫ/ОСНОВАНИЯ
ГЛАВА 14 ХИМИЯ УГЛЕРОДА
Ч. 15 ВОЛНЫ
Ч. 16 ЗВУК
16 ЗВУК
Ч. 17 ЭЛЕКТРОМАГНИТНЫЕ ВОЛНЫ
Ч. 18 СВЕТ
Ч. 19 ЭЛЕКТРИЧЕСТВО
ВСЕ ППТС
Уравнения балансировки
НАУЧНЫЙ МЕТОД
Справочная лаборатория
Виртуальная лаборатория: Использование научного метода
Деятельность: Научный метод
Шаблон заметок Корнелла
Правила безопасности Губки Боба
Апология физики 8 класса [3-е издание 1]
0 Набор0 Описание Это 3-е издание курса «Изучение мироздания с помощью физических наук» было полностью переосмыслено и переписано с учетом интересов вашего ученика. Это не то же самое, что 2-е издание, и содержит больше информации по физике. В тексте обсуждаются атомная структура, периодическая таблица, химические связи, реакции и энергия, движение, силы, энергия, волны и звук, свет, электричество и магнетизм, а также структура Земли, выветривание и атмосфера.
В тексте обсуждаются атомная структура, периодическая таблица, химические связи, реакции и энергия, движение, силы, энергия, волны и звук, свет, электричество и магнетизм, а также структура Земли, выветривание и атмосфера.
Этот курс разработан как последний курс естествознания, который учащийся изучает перед биологией в старших классах. Обычно мы рекомендуем его в качестве курса для 8-го класса, но учащиеся могут использовать его для своей курсовой работы в 9-м классе.
- Список материалов для лаборатории
Содержание
МОДУЛЬ 1: НАУКА — ОСНОВЫ
- Что такое наука
- Наука и техника
- Что такое физическая наука
- Научный процесс
- Наблюдения
- Эксперимент 1.1: наблюдения
- Формирование гипотез
- Проверка гипотез
- Эксперименты
- Анализ данных
- Подведение итогов
- Научные теории и законы
- Наука не доказывает
- Когда научный метод невозможен
- Выводы
- Модели
- Измерение и обработка данных
- Метрическая система
- Масса
- Длина
- Том
- Время
- Температура
- Преобразование единиц
- Организация и представление научных данных
- Таблицы данных
- Анализ данных с помощью графиков
- Гистограммы
- Круговые диаграммы
- Линейные графики
- Ты занимаешься наукой
- Эксперимент 1.
2: практика сбора и анализа данных с помощью маятников
- Подведение итогов
- Ответы на вопросы «Самостоятельно»
- Учебное пособие по модулю 1
МОДУЛЬ 2: ХИМИЧЕСКИЕ СВОЙСТВА И СОСТОЯНИЯ ВЕЩЕСТВА
- Классификация вещества
- Чистые вещества и смеси
- Чистые элементы и соединения
- Смеси
- Твердые тела, жидкости и газы
- Другие состояния вещества
- Кинетическая теория материи
- Твердые вещества
- Жидкости
- Газы
- Эксперимент 2.1: Диффузия при различных температурах
- Металлы и неметаллы
- Свойства материи
- Физические свойства
- Внешний вид и запах
- Проводимость
- Плотность
- Эксперимент 2.2: изучение различных плотностей
- Твердость
- Пластичность
- Вязкость
- Температуры плавления и кипения
- Химические свойства
- Воспламеняемость
- Реактивность
- Изменения в материи
- Физические изменения
- Изменения объема и плотности
- Вы занимаетесь наукой: активность по изменению объема и плотности
- Фазовые изменения
- Изменения растворимости
- Химические изменения
- Изменение цвета
- Производство газа
- Формирование твердого тела
- Эксперимент 2.
3: изменения в материи
- Подведение итогов
- Ответы на вопросы «Самостоятельно»
- Учебное пособие по Модулю 2
МОДУЛЬ 3: ХИМИЯ — АТОМНАЯ СТРУКТУРА И ПЕРИОДИЧЕСКАЯ ТАБЛИЦА
- История атома
- Древние атомные модели
- Атомная теория Дальтона
- Модель атома Томсона
- Сливовый пудинг Модель
- Атомная модель 9 Резерфорда0277
- Структура атомов
- Субатомные частицы
- Атомный номер и массовое число
- Изотопы
- Современная атомная теория
- Модель атома Бора
- Электронное облако или квантово-механическая модель
- Электронные орбитали
- Эксперимент 3.1: создание трехмерных моделей атомов
- Организующие элементы: Периодическая таблица
- Периодическая таблица Менделеева
- Эксперимент 3.2: создание периодической таблицы
- Группы и периоды
- Современная периодическая таблица
- Репрезентативные группы
- Щелочные металлы
- Щелочноземельные металлы
- Группа Бор
- Углеродная группа
- Углеродная группа
- Группа азота
- Кислородная группа
- Галогены
- Дворянские газы
- Подведение итогов
- Ответы на вопросы «Самостоятельно»
- Учебное пособие по Модулю 3
[ В остатке показаны только темы основного модуля.




 2: практика сбора и анализа данных с помощью маятников
2: практика сбора и анализа данных с помощью маятников 3: изменения в материи
3: изменения в материи