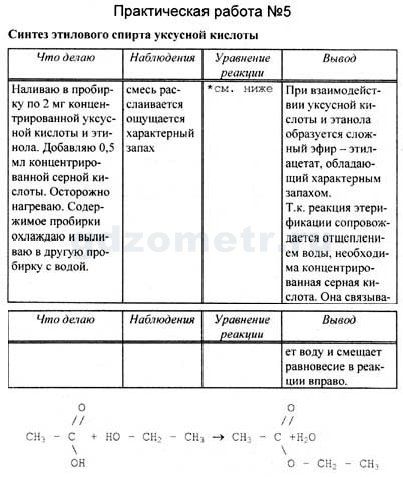
№ п/п | Название работы | Оборудование и реактивы |
1 | Приемы обращения с лабораторным оборудованием | Оборудование: Штатив, спиртовка, лабораторная посуда. |
2 | Очистка загрязненной поваренной соли | Оборудование: смесь песка с солью, 2 стаканчика, стеклянная палочка, промывалка с водой, фильтр, воронка, спички, спиртовка, зажим, чашка для выпаривания. |
2 | Анализ почвы и воды | Оборудование: две пробирки, воронка, бумажный фильтр, стеклянная палочка, предметное стекло, спиртовка, стеклянный цилиндр с водой, пробка, универсальная индикаторная бумага. |
3 | Наблюдение за горящей свечой | Оборудование: Свеча, резиновая груша, пробирки, предметное стекло, 2 химических стакана разного размера. Реактивы: Известковая вода. |
4 | Приготовление растворов | Оборудование: Мерный цилиндр, коническая колба, лабораторные весы. Реактивы: Сахар, вода. |
5 | Признаки химических реакций | Оборудование: спиртовка, штатив с пробирками. Реактивы: медная проволока, H2SO4, HCl, роданид калия (KSCN), мел (CaCO3), FeCl3, Na2СO3, СaCl2. |
6 | Ионные реакции и условия их протекания | Оборудование и реактивы: пробирки, растворы сульфата меди (II), гидроксида натрия, хлорида бария, карбоната натрия, азотной кислоты, серной и соляной кислот, фенолфталеин. |
7 | Свойства кислот, оснований, оксидов и солей | Оборудование: штатив с пробирками. Реактивы: HCl, NaOH, Na2CO3, AgNO3, BaCl2, H2SO4, FeCl3, фенолфталеин. |
8 | Решение экспериментальных задач | Оборудование: спиртовка, штатив с пробирками. Реактивы: KCl, MgSO4, Zn, PbNO3, BaCl2, H2SO4 |
Практическая работа №1.
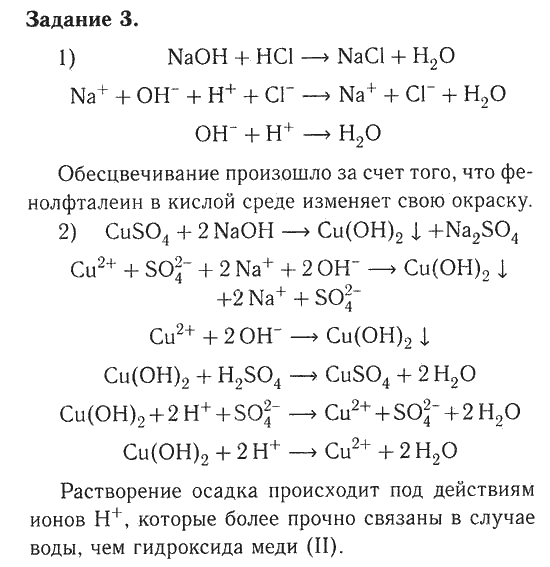 Знакомство с лабораторным оборудованием. Правила техники безопасности —
Знакомство с лабораторным оборудованием. Правила техники безопасности —- 7 класс
- 8 класс
- 9 класс
Цель: изучить основные виды химической посуды, лабораторного оборудования и правил работы с ними.
Знакомство с лабораторным штативом. Устройство лабораторного штатива.
Объясните, почему подставка штатива изготавливается массивоной?
Для увеличения устойчивости.
Задание 1. Знакомство с устройсвом штатива.
Снимите с установленного на столе штатива лапку и кольцо. Для этого ослабьте винст крепления муфты со стержнем и, поднимая муфту с лапкой или кольцом вверх, снимите ее со стержня штатива. Освободите лапку и кольцо от муфты: поверните против часовой стрелки винт, удерживающий лапку и кольцо, и выньте их из муфты. Наденьте муфту на стержень штатива так, чтобы винт, закрепляющий ее, был слева от стержня, а стержни лапки или кольца укреплялись бы таким образом, чтобы их поддерживал не только винт, но и муфта
Почему стержни лапок и колец располагаются сверху муфты?
Чтобы они не упали, если будут плохо закреплены.
Задание 2. Пользование штативом.
1. Почему закрепленная в лапке пробирка должна сравнительно свободно поворачиваться?
Чтобы при нагревании стекло не лопнуло.
2. Заполните таблицу 3.
Химическая посуда.
| НАЗВАНИЕ | РИСУНОК | МАТЕРИАЛ | НАЗНАЧЕНИЕ |
| мерный цилиндр | стекло | для отмеривания определеного объема жидкости | |
| реторта | стекло | для перегонки жидкостей | |
| круглодонная колба | стекло | проведение реакция, перегонка жидкостей | |
| плоскодонная колба | стекло | для проведения химических реакций без нагревания | |
| коническая колба | стекло | для жидкостей | |
| пробирка | стекло | для проведения реакций с небольшим количеством реактивов | |
| химический стакан | стекло | для жидкостей | |
| конусная воронка | стекло | для переливания жидкостей | |
| чашка | фарфор | для выпаривания растворов, измельчения твердых веществ |
3.
Так как стекло прочное, химически стойкое, инертное. С ним не взаимодействует большинство химических веществ.
4. Назовите лабораторное оборудование.
Наблюдение и эксперимент как методы изучения естествознания и химииПрактическая работа №2. Наблюдение за горящей свечой, устройство и работа спиртовки
Исследование химических изменений — Каковы некоторые признаки химических изменений?
Жанин Солсбери, Средняя школа Роббинсдейла, Роббинсдейл, Миннесота, на основе оригинальной деятельности McDougal Littell Science, Matter and Energy, стр. 47
Профиль автора
Резюме
Это открытая лаборатория, которую можно выполнить примерно за 15-20 минут с помощью нескольких бытовых материалов. Он эффектно, но просто иллюстрирует изменение цвета и образование газа (пузырьков) в результате химического изменения.
Цели обучения
Навыки:
1. Следующие пошаговые инструкции
2. Следуя последовательности
3. Измерение
4. Рабочая совместная работа
1. Знание и понимание.
2. Синтез и оценка.
3. Метапознание.
Ключевые понятия:
Существует пять признаков химического изменения:
1. Изменение цвета
2. Появление запаха
3. Изменение температуры
4. Выделение газа (образование пузырьков)
5. Осадок (образование твердого вещества) )
. Это задание подходит для нескольких учащихся до 30-35 лет. Единственным ограничением будет место на столе и градуированные цилиндры. Все остальное можно купить в продуктовом магазине. Лаборатория — это исследование, и ее можно использовать для ознакомления с концепциями химических изменений. Его также можно использовать для демонстрации химических изменений цвета и пузырьков. Это лабораторная работа, на выполнение которой уходит примерно 15-20 минут учебного времени. Также потребуется 15-20 минут для записи наблюдений и ответов на вопросы, а также дополнительное время для настройки и очистки. Время, необходимое для этого, будет зависеть от количества детей, выполняющих лабораторную работу. Это можно делать индивидуально или в группах по два человека. При необходимости это можно делать и в больших группах, но намного веселее с 1-2 учениками. Единственное специальное оборудование, которое понадобится, — это градуированные цилиндры. Полезно, если учащиеся изучали физические изменения, но это не обязательно. Эту лабораторную работу можно использовать как упреждающий набор или как пример(ы) химических изменений в материалах. Дети могут выполнить лабораторную работу, а затем узнать, почему произошли изменения, или они могут использовать ее для демонстрации усвоенных понятий. Это упражнение можно использовать практически в любых условиях.
Его также можно использовать для демонстрации химических изменений цвета и пузырьков. Это лабораторная работа, на выполнение которой уходит примерно 15-20 минут учебного времени. Также потребуется 15-20 минут для записи наблюдений и ответов на вопросы, а также дополнительное время для настройки и очистки. Время, необходимое для этого, будет зависеть от количества детей, выполняющих лабораторную работу. Это можно делать индивидуально или в группах по два человека. При необходимости это можно делать и в больших группах, но намного веселее с 1-2 учениками. Единственное специальное оборудование, которое понадобится, — это градуированные цилиндры. Полезно, если учащиеся изучали физические изменения, но это не обязательно. Эту лабораторную работу можно использовать как упреждающий набор или как пример(ы) химических изменений в материалах. Дети могут выполнить лабораторную работу, а затем узнать, почему произошли изменения, или они могут использовать ее для демонстрации усвоенных понятий. Это упражнение можно использовать практически в любых условиях.
Предмет : Химия:Общая химия
Тип ресурса : Виды деятельности: Лабораторная работа
Уровень : Средний (6-8)
Описание и учебные материалы
Материалы, необходимые для 1 эксперимента:
1. 1 градуированный цилиндр
2. Вода
3. 2 Прозрачные пластиковые чашки
4. 2 Eyedroppers
5. Иодин или Lugol’s Solder’s
6. Кукурузный крахмал
7. 2 ложки (пластиковые)
8. 1 таблетка витамина С
Процедура:
1. Отмерьте 80 мл воды и налейте ее в одну из чашек.
2. Добавьте три полные пипетки раствора йода. Запишите свои наблюдения.
3. Добавьте одну ложку кукурузного крахмала в раствор йода и перемешайте.
4. Отмерьте 50 мл воды и налейте ее во вторую чашку.
5. Используя чистую пипетку, добавьте 4 полные пипетки раствора йода/кукурузного крахмала во вторую чашку.
6. Бросьте таблетку витамина С во вторую чашку и перемешайте жидкость чистой ложкой, пока таблетка не растворится. Запишите свои наблюдения.
Что вы думаете?
1. Какие изменения вы заметили в первой чашке? Во второй чашке?
2. Как вы думаете, произошли ли химические изменения? Почему или почему нет.
Задание: Опишите некоторые химические изменения, происходящие в вашем доме или школе.
Ссылка:
McDougal Littell Science, Matter and Energy, Copyright 2005, McDougal Littell, подразделение Houghton Mifflin Company, pg. 47
Учебные заметки и советы
Советы: Вы можете использовать йод из любой аптеки. Только будьте осторожны, так как он окрашивается и, вероятно, не сойдет с одежды. Старые мужские рубашки для взрослых хорошо подходят в качестве лабораторных халатов, и их можно приобрести в секонд-хендах по очень разумной цене. Если вы используете раствор Люголя, добавьте достаточно, чтобы раствор стал темно-желтым/оранжевым. Простой йод будет темно-красным.
Только будьте осторожны, так как он окрашивается и, вероятно, не сойдет с одежды. Старые мужские рубашки для взрослых хорошо подходят в качестве лабораторных халатов, и их можно приобрести в секонд-хендах по очень разумной цене. Если вы используете раствор Люголя, добавьте достаточно, чтобы раствор стал темно-желтым/оранжевым. Простой йод будет темно-красным.
Возможные ответы на Что вы думаете?
Цвет изменился с желтого/оранжевого, красного на сине-черный в первой чашке. Во второй чашке изменился цвет и образовались пузырьки. Да; образовались новые вещества, о чем свидетельствуют изменения цвета и пузырьки. Некоторыми признаками химического изменения являются изменение цвета и образование пузырьков. Пять условий химического изменения: изменение цвета, образование осадка, образование газа, изменение запаха, изменение температуры.

Проблема: приготовление пищи, образование ржавчины, образование потускнения на дверных ручках, сжигание топлива для обогрева, потускневший пенни.
Оценка
Оценка может быть формальной или неформальной. Учащиеся могут написать ответы на вопросы в своих научных журналах или на листе бумаги, чтобы сдать его. Они также могут рассказать о своих наблюдениях в небольших группах или в обсуждениях в большом классе.
Стандарты
1) 6.I.A.1 Учащийся будет различать научные данные и личное мнение.
2) 6.I.A.4 Учащийся будет определять научные факты, законы и теории.
3. 6.I.B.2 учащийся будет различать наблюдение, предсказание и вывод.
4. 6.II.B.1. Студент будет определять химические и физические изменения.
5. 6.II.B.2 Учащийся заметит, что вещества химически реагируют с другими веществами с образованием новых веществ с другими характерными свойствами.
Подробнее MnSTEP Деятельность »
Материя состоит из мельчайших частиц
Обзор урока для учителей
Посмотрите видео ниже, чтобы узнать, что вы и ваши ученики будете делать на этом уроке.
Идентификатор Youtube: Ll2ao9Irwgg
Загружаемые файлы:
План урока (PDF) | Лист активности учащихся (PDF) | Студенческое чтение (PDF) | История учителя (PDF) | Подключения к NGSS (PDF)
Учащиеся разработают модель, описывающую, что материя состоит из крошечных частиц, слишком маленьких, чтобы их можно было увидеть. Студенты будут использовать модель для описания различий в притяжении между частицами твердого тела, жидкости и газа. Наконец, учащиеся будут использовать свои модели твердых тел, жидкостей и газов, чтобы объяснить свои наблюдения на уроке.
Ключевые понятия- Вещество на Земле находится в твердом, жидком или газообразном состоянии.
- Твердые тела, жидкости и газы состоят из мельчайших частиц, называемых
- В твердом теле частицы сильно притягиваются друг к другу. Они расположены близко друг к другу и вибрируют в одном положении, но не проходят мимо друг друга.

- В жидкости частицы притягиваются друг к другу, но не так сильно, как в твердом теле. Частицы жидкости находятся близко друг к другу, всегда движутся и могут скользить друг относительно друга.
- В газе частицы очень слабо притягиваются друг к другу. Они находятся очень далеко друг от друга по сравнению с частицами в твердом теле или жидкости и постоянно движутся. Частицы не взаимодействуют друг с другом, а просто ударяются и отскакивают друг от друга при столкновении.
Выравнивание NGSS
- NGSS 5-PS1-1: Разработайте модель, описывающую, что материя состоит из частиц, слишком маленьких, чтобы их можно было увидеть.
- Учащиеся знакомятся с идеей о том, что материя состоит из мельчайших частиц, называемых атомами и молекулами.
- Учащиеся наблюдают за цельнометаллическим молотком и гвоздем и просматривают анимацию молекулярной модели частиц в твердом теле.
- Учащиеся сжимают гибкую пластиковую бутылку с воздушным шаром сверху бутылки, чтобы разработать модель частиц газа.

- Студенты также пытаются сжать бутылку, наполненную водой, чтобы разработать модель частиц жидкости.
- Студенты смотрят короткую анимацию, иллюстрирующую невероятно крошечные размеры атомов и молекул.
- Наконец, студенты выдвигают аргумент, что, хотя горка крема для бритья сохраняет свою форму, она не является твердой, и что хотя песок принимает форму контейнера, он не является жидкостью.
Распечатайте лист с заданиями учащегося и раздайте по одному учащемуся, если это указано в задании. Рабочий лист будет служить компонентом оценки плана урока 5-E.
БезопасностьУбедитесь, что вы и ваши ученики носите правильно подобранные защитные очки.
Уборка и утилизация Напомните учащимся мыть руки после выполнения заданий.
Сохраните бутылки и песок для будущего использования. Все другие обычные бытовые или школьные материалы можно сохранить или утилизировать обычным образом.
- Молоток, гвоздь и дерево
- Гибкая пластиковая бутылка из-под содовой (18-20 унций) с крышкой
- Воздушный шар
Примечание: гибкие пластиковые бутылки из-под газировки работают лучше, чем одноразовые бутылки из-под воды , потому что бутылки из-под воды часто не очень гибкие и имеют тенденцию полностью ломаться при сжатии.
Материалы для демонстрации EXTRA EXTEND- Крем для бритья
- Маленькая пластиковая или бумажная тарелка
- Песок
- 2 прозрачных пластиковых стаканчика
Engage 1. Продемонстрируйте, что молоток представляет собой твердое тело.
Скажите учащимся, что все, что они могут увидеть и потрогать, называется материей . Объясните, что вся материя на Земле существует в виде твердого тела, жидкости или газа и что все твердые тела, жидкости и газы состоят из мельчайших частиц, называемых атомов и молекул .
Скажите учащимся, что атом — это наименьший строительный блок материи, а молекула — это два или более атомов, соединенных вместе. Атомы и молекулы настолько малы, что мы их не видим. Ученые используют модели, чтобы попытаться понять поведение атомов и молекул и помочь объяснить свойства материи.
Примечание: Несмотря на то, что атомы и молекулы разные, для целей этого урока они оба будут представлены одинаково в виде круга или сферы. В последующих уроках они будут показаны на разных моделях.
Материалы- Молоток
- Гвоздь
- Дерево
- Используйте молоток, чтобы частично вбить гвоздь в кусок дерева.
- Поднимите молоток и объясните учащимся, что твердые твердые материалы, такие как металл молотка, состоят из атомов, которые сильно притягиваются друг к другу, поэтому они крепко держатся друг за друга.
Примечание: Если вы не хотите забивать гвоздь в дерево, просто слегка постучите молотком по твердой, прочной, небьющейся поверхности, например по столу или стулу.
Показать анимацию Частицы твердого тела.
Объясните, что частицы в твердом теле сильно притягиваются друг к другу и колеблются на месте. Сильное притяжение между частицами удерживает их близко друг к другу и делает твердые тела, такие как металл в молотке, твердыми.
Раздайте каждому учащемуся рабочий лист (PDF) .
Учащиеся записывают свои наблюдения и отвечают на вопросы о задании в листе задания.
Исследовать
2. Предложите учащимся посмотреть на свою «пустую» бутылку, а затем поэкспериментировать с воздушным шаром.
Вопрос для исследования: действительно ли пустая бутылка пуста?
- Гибкая пластиковая бутылка из-под содовой (18–20 унций) с крышкой
- Воздушный шар
Примечание: Одноразовые пластиковые бутылки для воды не подходят, потому что они не очень гибкие и имеют тенденцию полностью разрушаться при сжатии.
- Предложите учащимся посмотреть на открытую бутылку и взять ее в руки.
- Если в бутылке нет жидкости, то является ли она полностью пустой?
Возможно. - В бутылке вообще что-нибудь есть?
Да, в бутылке есть воздух.
Объясните, что в бутылке есть воздух и что воздух состоит из различных газов, таких как кислород, азот и углекислый газ, которыми мы дышим каждый день. Объясните, что газ состоит из мельчайших частиц. Скажите учащимся, что газ сильно отличается от твердого тела.
Скажите учащимся, что если они все еще сомневаются в том, что в бутылке что-то есть, они могут надеть на нее воздушный шар и посмотреть, что произойдет, когда они сожмут бутылку.
- Аккуратно наденьте шарик на горлышко бутылки.
- Держите бутылку и сжимайте ее до тех пор, пока вы не сможете сжимать ее дальше.

- Что происходит с шариком, когда вы сжимаете бутылку?
Баллон расширяется.
- Как вы думаете, что произошло с молекулами газа, когда вы сжали бутылку и шарик расширился?
Молекулы газа должны были попасть из баллона в воздушный шар.
Объяснить 3. Покажите анимацию и обсудите, как использование воздушного шара показывает, что в бутылке должно быть что-то.
Показать анимацию Частицы газа в бутылке.
Объясните, что сферы представляют собой частицы газа. Объясните, что частицы газа не сильно притягиваются друг к другу, а просто ударяются друг о друга и отскакивают. Частицы также намного дальше друг от друга, чем в твердом теле.
Объясните, что когда бутылку сжимают, молекулы газа перемещаются из бутылки в воздушный шар, заставляя его расширяться.
4. Попросите учащихся сжать бутылку с крышкой.
Попросите учащихся сжать бутылку с крышкой. Вопрос для исследования: Можно ли заставить молекулы газа сблизиться?
Материалы для каждой группы
- Гибкая пластиковая бутылка из-под содовой (18–20 унций) с крышкой
- Снимите баллон с флакона и плотно закройте крышкой.
- Сожмите бутылку.
- В бутылке находятся молекулы газа. Когда крышка плотно закрыта, вы смогли сжать бутылку?
Да - Вы не можете сжать твердое тело, такое как металл или камень, так что же такого в молекулах газа, что позволяет вам сжимать его?
Молекулы газа находятся очень далеко друг от друга, поэтому их можно сжать в меньшее пространство.
Показать анимацию Наблюдение за газом в бутылке.
Объясните, что с закрытой крышкой бутылку все еще можно сжать, потому что молекулы газа имеют большое пространство между собой и могут быть сжаты.
Исследовать 5. Предложите учащимся исследовать бутылку с водой.
Вопрос для исследования: Можно ли заставить молекулы жидкости сблизиться?
Материалы для каждой группы
- Гибкая пластиковая бутылка из-под содовой (18–20 унций) с крышкой
- Вода
Процедура
- Наполните бутыль до самого верха и плотно закройте бутылку крышкой.
- Сожмите бутылку.
Ожидаемые результаты
Бутылку очень трудно сжать. Он почти кажется твердым.
Спросите учащихся:
- Удалось ли вам сжать бутылку так сильно, как когда в ней был газ?
№ - Сдавив бутылку с газом и бутылку с жидкостью, как вы скажете, частицы жидкости ближе друг к другу или дальше друг от друга, чем частицы газа?
Ближе друг к другу
Объяснить 6.
 Покажите анимацию и обсудите движение и расположение частиц жидкости.
Покажите анимацию и обсудите движение и расположение частиц жидкости. Показать анимацию Жидкость в бутылке.
Объясните, что частицы жидкости притягиваются гораздо сильнее, чем частицы газа, и что они гораздо ближе друг к другу. Они почти так же близко друг к другу, как твердое тело, но они могут скользить друг мимо друга. Они настолько близко друг к другу, что их очень трудно сжать.
7. Покажите анимацию и сравните движение и расположение частиц твердого тела, жидкости и газа.
Показать анимацию Сравнение твердого тела, жидкости и газа.
- Твердое тело: Объясните, что в твердом теле частицы сильно притягиваются друг к другу, поэтому они находятся близко друг к другу. Частицы могут двигаться в своих фиксированных положениях, но не могут скользить друг мимо друга.
- Жидкость: В жидкости частицы также притягиваются друг к другу, но не так сильно, как в твердом теле.
 Частицы находятся близко друг к другу, постоянно движутся и могут скользить друг мимо друга.
Частицы находятся близко друг к другу, постоянно движутся и могут скользить друг мимо друга. - Газ: В газе частицы почти не притягиваются друг к другу. Они находятся очень далеко друг от друга и просто ударяются и отскакивают друг от друга, постоянно перемещаясь.
Расширить 8. Покажите анимацию и обсудите, насколько крошечными являются атомы и молекулы.
Учащихся познакомили с идеей о том, что вещество, твердое, жидкое или газообразное, состоит из мельчайших частиц, называемых атомами и молекулами. Объясните учащимся, что иллюстрации и анимации атомов и молекул, которые они видели, являются моделями, используемыми для представления атомов и молекул. Объясните, что реальный размер атомов и молекул невероятно мал, в триллионы раз меньше, чем точки или сферы, которые мы используем для их представления.
На самом деле атомы и молекулы настолько малы, что миллионы из них поместились бы на месте одной точки в конце предложения.
Показать анимацию Атомы маленькие — очень маленькие.
Скажите учащимся, что анимация рассказывает о том, насколько невероятно малы атомы и молекулы. Он основан на количестве молекул воды в столовой ложке воды, что составляет около 600 000 000 000 000 000 000 000 — около 600 миллиардов триллионов, поэтому они очень маленькие.
Extra Extend 9. Подумайте, являются ли крем для бритья и песок твердыми, жидкими или газообразными.
Сообщите учащимся, что в некоторых книгах и других источниках состояния материи могут быть определены более просто следующим образом:
- Твердое тело – сохраняет свою форму даже без контейнера
- Жидкость – принимает форму контейнера
- Газ – Распределяется для заполнения любого контейнера
Вопрос для исследования: Как классифицировать вещество, которое не соответствует этим простым определениям твердых тел, жидкостей и газов?
Демонстрационные материалы
- Песок
- 2 прозрачных пластиковых стаканчика
- 1 банка крема для бритья
- 1 небольшая пластиковая или бумажная тарелка
- Насыпьте от ¼ до ½ стакана песка в один пластиковый стаканчик.

- Нанесите небольшое количество крема для бритья на бумажную тарелку для демонстрации.
- Осторожно пересыпьте песок из одной чашки в другую.
- Принимает ли песок форму чаши?
Да. - Значит ли это, что песок является жидкостью?
Нет. Каждый кусок песка является твердым, но эти кусочки настолько малы, что когда вы их насыпаете, они принимают форму контейнера. Песок — твердое тело, но ведет себя как жидкость, потому что его крошечные кусочки принимают форму контейнера, в который вы его насыпаете.
1. Покажите учащимся горку крема для бритья.
Спросите учащихся:- Если вы не прикасаетесь к нему, сохраняет ли холмик крема для бритья свою форму без контейнера?
Да - Значит ли это, что это твердое тело?
Нет.






.jpg)
 Частицы находятся близко друг к другу, постоянно движутся и могут скользить друг мимо друга.
Частицы находятся близко друг к другу, постоянно движутся и могут скользить друг мимо друга.