Первоначальные химические понятия и законы (химический диктант) | Учебно-методический материал по химии (8 класс) на тему:
8 класс Первоначальные химические понятия
(химический диктант)
Химия – наука о веществах, составе и свойствах веществ, а также превращениях между ними.
Вещество- материя, из которой состоит физическое тело.
Химический элемент –определенный вид атомов, имеющих одинаковый размер, массу и свойства.
Атом- наименьшая частица вещества, являющаяся носителем его свойств.
Молекула –частица, образованная из двух или большего числа атомов и способная к самостоятельному существованию.
Простое вещество- вещество, состоящее из атомов одного химического элемента.
Сложное вещество- вещество, состоящее из атомов разных химических элементов.
Относительная атомная масса (Ar)- величина, которая показывает, во сколько раз масса атома химического элемента больше атомной единицы массы (1/12 массы атома углерода).
Относительная молекулярная масса(Mr) – величина, которая показывает, во сколько раз масса молекулы больше атомной единицы массы (1/12 массы атома углерода).
Ион- это положительно или отрицательно заряженная частица, образованная из атома химического элемента в результате отдачи или присоединения электронов. Положительно заряженный ион- катион, отрицательно заряженный ион – анион.
Химическая связь- такое взаимодействие между атомами, которое связывает их в молекулы, ионы, кристаллы.
- Ионная связь-связь, возникающая между ионами. (за счет перехода электронов от атома металла к атому неметалла):NaCl, CaBr2, K2O и др.
- Ковалентная неполярная связь — связь, возникающая между атомами одного и того же химического элемента – неметалла (О2 , N2, Cl2, Br2, O3 и т.п.)
- Ковалентная полярная связь — связь, возникающая между атомами разных неметаллов (СО2, h3O, Nh4).
- Металлическая связь — связь, возникающая между атомами и ионами металлов за счет обобществленных электронов (Сu, Al, Na, K и др.
 ).
).
Электроотрицательность- способность атома химического элемента притягивать к себе общие электронные пары от атомов других химических элементов.
Степень окисления – условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что соединения состоят только из ионов.
Классификация веществ:
— простые (металлы и неметаллы)
— сложные (оксиды, основания, кислоты, соли).
- Оксиды- сложные вещества, состоящие из двух химических элементов, один из которых кислород со степенью окисления -2. ( ЭхОу-2)
- Основания- сложные вещества, состоящие из катионов металла и гидроксид-ионов ОН. (Me+x(OH)x)
- Кислоты — сложные вещества, состоящие из катионов водорода Н+ и анионов кислотных остатков.
- Соли — сложные вещества, состоящие из катионов металла и анионов кислотных остатков.
Моль-такое количество вещества, в котором содержится 6∙1023 частиц этого вещества (атомов, молекул или ионов)
Молярная масса(M)- масса 1 моль вещества, численно равна относительной молекулярной массе, но в отличие от нее имеет единицы измерения. [M]=[г/моль].
[M]=[г/моль].
Молярный объем (Vm)- объем газа количеством вещества 1 моль, измеренный при нормальных условиях ( t= 0oC или 273К, р=101,3 кПа, 1 атм или 760мм рт. ст.). Vm= 22,4 л/моль
Химическая реакция — явление, в результате которого из одних веществ образуются другие вещества, при этом изменяется состав и свойства веществ.
- Реакции разложения- реакции, в результате которых из одного сложного вещества образуются нескольно простых или сложных веществ( АВ= А+В)
- Реакции соединения — реакции, в результате которых из нескольких простых или сложных веществ образуется одно сложное. (А+В=АВ).
- Реакции замещения – реакции, в результате которых атомы простого вещества замещают один или несколько атомов в сложного вещества ( А +ВС= АС +В)
- Реакции обмена — реакции, в результате которых атомы сложных веществ обмениваются своими составными частями (АВ+ CD=AD +CB)
Физические явления- явления, при которых могут изменяться размеры, форма тел и агрегатное состояние веществ, при этом состав их остается постоянным.
Химическое уравнение – условная запись химической реакции с помощью химических формул и математических знаков.
Закон сохранения массы веществ (1748г М.В. Ломоносов, 1789г А.Лавуазье): масса веществ , вступивших в химическую реакцию, равна массе образовавшихся веществ.
Закон постоянства состава (1808г Ж. Пруст)-вещества молекулярного строения имеют постоянный количественный и качественный состав, не зависящий от способа их получения.
Периодический закон (1861 г Д.И.Менделеев) –свойства химических элементов и их соединений находятся в периодической зависимости от зарядов ядер их атомов.
химия 8 — 1 четверть
Уважаемые ребята! Если
Вы пропустили урок химии или желаете получить дополнительную
информацию по изученной теме, приглашаю Вас на виртуальные уроки,
которые помогут Вам основательно разобраться в химических явлениях и
закрепить Ваши знания при помощи предлагаемых лекций, тестов,
анимационных опытов. В таблице отражены основные темы за курс химии 8 класса в 1 четверти. Для того, чтобы просмотреть, изучить, повторить определенную тему, наведите курсор на тему и перейдите по ссылке. Тема №1 Первоначальные химические понятия
|
Класс 8 Химия Примечания | Физика Wallah
Главы по химии для 8 класса
Главы по химии для 8 класса
Химия является предметом понятий и реакций. Основы химии начинаются с 8 класса. Химия 8 класса строит ваши основы, которые требуются в старших классах. Чтобы укрепить ваши знания в области химии, академическая группа Physics Wallah подготовила структурированный учебный материал по химии для 8 класса.
Химия класса 8 состоит из теории деталей с добавленными решенными вопросами и MCQ. Класс 8 Наука состоит из 17 глав, из которых 7 глав относятся к химии. Решайте вопросы из учебника NCERT с помощью Physics Wallah 9.0009 Решения NCERT для класса 8 по естественным наукам

Химия класса 8 очень интересна, вы поймете атом и молекулы, символы и различные типы реакций. Глава «Углерод и его соединения» даст фундаментальное представление об органической химии. В этой главе объясняются структура и функции углерода и его изотопов.
- Металлы и неметаллы
В этой главе вы узнаете, какими свойствами обладают металлы и неметаллы. Реакции металлов и неметаллов. Как идентифицировать металлы по их физическим и химическим свойствам.
- Горение и пламя
Все мы знаем о пламени, в этой главе рассказывается очень интересная деталь о пламени. Характеристика пламени поможет вам определить, каковы разности температур в слоях пламени.
- Углерод и его соединения
Одна из важных глав химии класса 8. Начните знакомство с основами органической химии с этой главы и поймите химические и физические свойства углерода.
- Синтетическое волокно
Большинство вопросов, задаваемых на школьном экзамене, взяты из этой главы. В этой главе объясняется, как производится синтетическое волокно и каковы свойства синтетического волокна.
- Уголь и нефть
Как уголь производят на земле. Химические и физические свойства нефти.
- Кислотное основание и соль
Поймите, как идентифицировать кислотное основание и соль. Каковы разные определения кислотного основания и соли. Это одна из важных глав химии 8 класса.
- Соединения и смеси элементов
Эта глава является одной из основных глав химии класса 8 и объясняет основы атомных молекул и несколько важных терминов.
Правильный подход к химии
Химия 8 класса состоит из очень важных тем, которые являются основами высшей химии. В 8 классе химии вы начнете строить основы предмета химии. Итак, начните с понимания структуры атома, узнайте, как это работает, задайте вопросы, почему, как, когда и попытайтесь найти ответ, учебник NCERT состоит из очень интересного примера химии класса 8, прочитайте все эксперименты и теории, упомянутые в учебнике.
Итак, начните с понимания структуры атома, узнайте, как это работает, задайте вопросы, почему, как, когда и попытайтесь найти ответ, учебник NCERT состоит из очень интересного примера химии класса 8, прочитайте все эксперименты и теории, упомянутые в учебнике.
Решите вопросы NCERT с помощью решений NCERT. Попробуйте найти вопросы, заданные в упражнении, и решить пример и выучить понятие, данное в классе 8 по химии. Академическая группа по физике Валлах подготовила главы по химии для 8 класса, которые являются частью науки для 8 класса. Мы добавили несколько дополнительных глав, которые дадут вам важные дополнительные знания по химии.
Советы по химии для 8 класса
- Начните готовить свои заметки, сделайте отдельные заметки для важных формул.
- Начните с запоминания символов химии, прочитайте периодическую таблицу, попробуйте запомнить символы атома, это будет очень полезно для старшего класса.
- Запомните атомный номер не менее 20 элементов таблицы Менделеева, это поможет вам в вопросах.

- Главы, такие как углерод и его соединения, кислотно-щелочное основание и соль, требуют дополнительной практики. Прочитайте части теории химии класса 8 по физике Уоллаха и решите все вопросы, данные в упражнении, это поможет вам подготовить прочную основу химии класса 8 для предстоящего урока. .
- Решите упражнение из учебника NCERT, и для справки вы можете воспользоваться помощью решений NCERT для науки 8 класса.
- Прочтите академический ресурс, доступный в Physics Wallah. В Physics Wallah вы получите заметки по химии, формул по химии , вопросы по химии и онлайн-тест по химии для класса 8 , так что ознакомьтесь с другим ресурсом, чтобы преуспеть во всех вступительных экзаменах.
Часто задаваемые вопросы (FAQ)
Q1. Почему повторный материал важен для химии 8 класса?
Ответ. Заметки о пересмотре необходимы для поддержки теоретического понимания темы химии и подготовки к экзамену.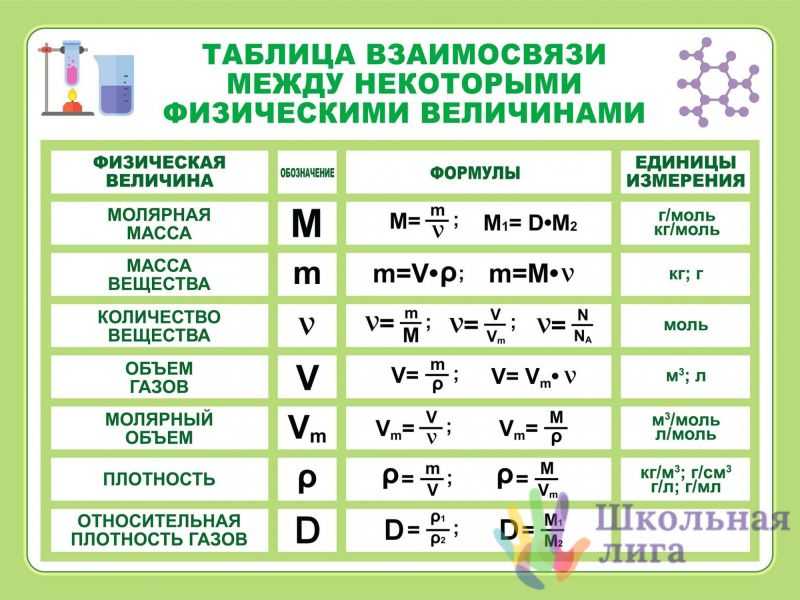
В видео наши эксперты делятся советом или примером применения полезных концепций химии в реальной жизни. Из этих видеороликов вы можете получить более четкое представление о концепции химии NCERT Class 8, о которой вы можете забыть. Благодаря этим пересмотрам вы полюбите химию и сможете интересно давать ответы.
Q2. Сколько практических тестов по химии в 8 классе я должен сдать?
Ответ. Пройди несколько практических тестов и узнай, насколько ты справился с ними. Если вы набрали низкий балл, перейдите к исправлению образцов работ, смоделируйте контрольные работы и попробуйте решить упражнение по химии NCERT класса 8 для практики, а затем пересдайте тест. Берите столько, сколько тестируете, больше практикуйтесь, больше избавляйтесь от сомнений, но убедитесь, что улучшите свою слабую область с достаточным пересмотром.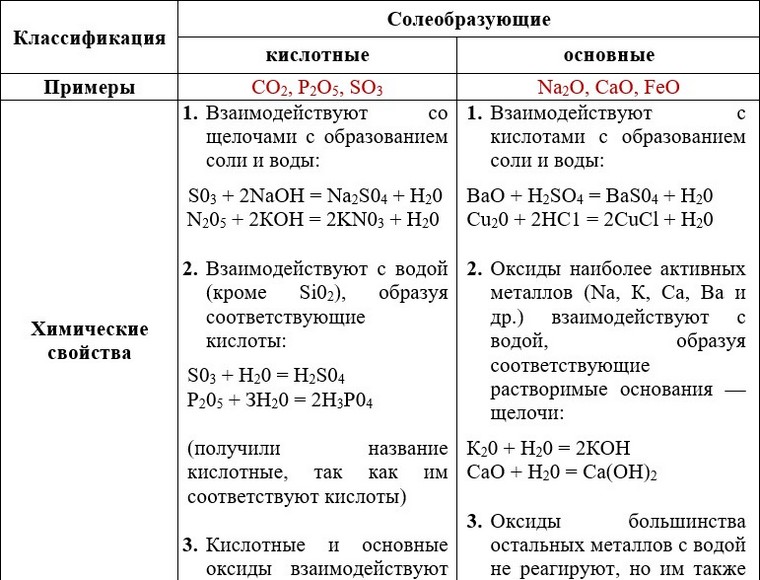
Q3. Как решать вопросы по химии в 8 классе?
Ответ. Прежде чем пытаться ответить на вопросы по химии для 8 класса, вы должны следовать следующим правилам, например.
- Прочитайте главу теоретически и убедитесь, что вы поняли концепцию, а затем сделайте заметки.
- При подготовке конспектов записывать все важные формулы и пункты.
- Попробуйте попрактиковаться на примерах, приведенных в учебнике химии NCERT для 8 класса.
- Не пользуйтесь калькулятором и не сверяйтесь с заметками при решении вопросов.
Q4. Как учащийся может использовать заметки по химии в 8 классе, чтобы получить хорошие оценки на экзамене в 8 классе?
Ответ. Физика Уолла подготовил заметки по химии для 8 класса, которые состоят из углубленной теории, подробно объясняющей все концепции и моменты, которые помогают учащимся построить прочную основу. Physics Wallah предоставляет вам все образцы работ, MCQ, которые помогут вам проверить свои концепции, а для школьного экзамена вы должны следовать решениям NCERT по химии для 8-го класса по Physics Wallah.
Q5. Будет ли просмотр видеоуроков по химии для 8 класса эффективнее чтения конспектов?
Ответ. Что ж, у каждого онлайн-обучения есть своя цель, и каждый ученик учится в соответствии со своими способностями. Видео уроки поддержат вас дальновидной ясностью в привлекательном формате. Чтение примечаний к главам поможет вам быстро прочитать важные понятия из каждой главы перед экзаменом или классным тестом.
Q6. Почему вы должны выбрать Physics Wallah?
Ответ. Учебные материалы по физике Wallah включают примечания к пересмотру, образцы статей и практические тесты. Образцы документов связаны с целью вашего экзамена. Заметки по химии подготовлены опытными учителями в соответствии с последней программой химии NCERT класса 8. Если у вас есть какие-либо сомнения в каком-либо вопросе, вы можете задать вопрос в разделе «Задать вопрос», наши специалисты ответят на ваши вопросы в ближайшее время.
CBSE Class 8 Chemistry Notes
GeeksforGeeks представляет CBSE Class 8 Chemistry Notes, которые основаны на последней программе, предписанной Центральным советом по образованию (CBSE). CBSE рекомендует книги NCERT для изучения во всех дочерних школах. Таким образом, заметки GeeksforGeeks по химии для 8-го класса разработаны и разработаны в соответствии с учебником NCERT по естественным наукам для 8-го класса таким образом, чтобы помочь учащимся более эффективно учиться и понимать каждую концепцию, охватываемую их учебной программой для 8-го класса. Эти заметки по химии помогут не только получить хорошие оценки в учебе, но и пригодятся при подготовке к различным конкурсным экзаменам, таким как NTSE и олимпиады.
К тому времени, когда ученики переходят в 8-й класс, они уже имеют некоторое представление об основах науки. Следовательно, приведенные ниже примечания к повторению химии для них основаны на концепциях, которые они уже изучили в классе 6 и классе 7. Здесь важные главы, такие как металлы и неметаллы, уголь и нефть и т.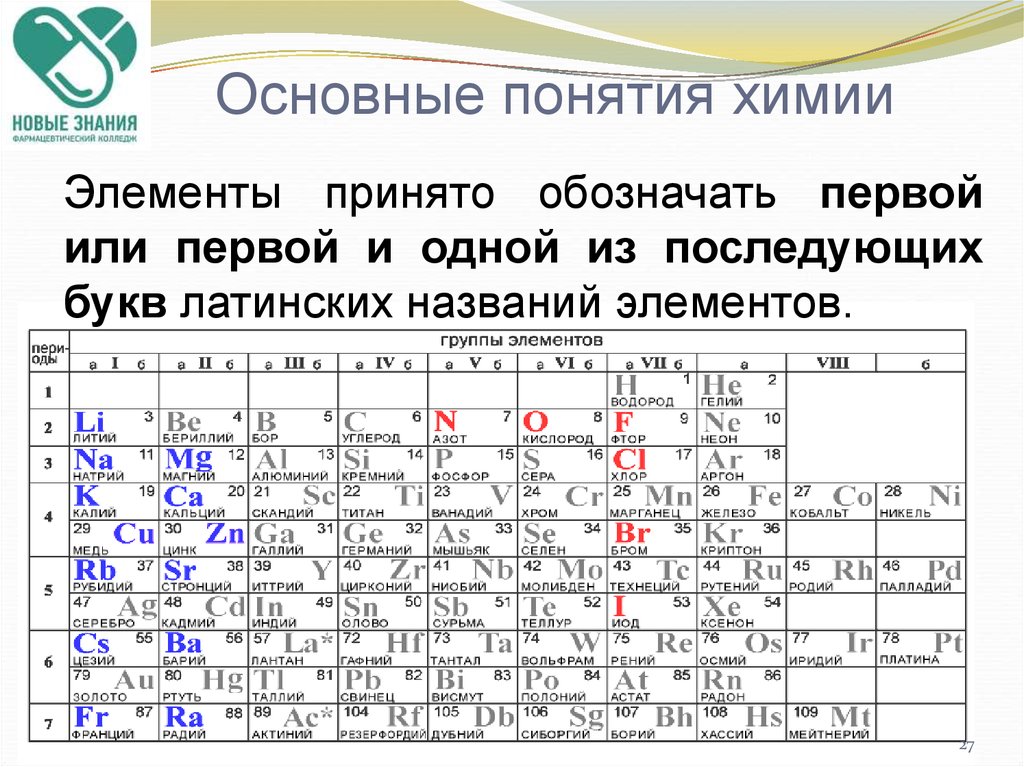 д., представлены в простой форме для тщательного изучения. обучения, а также для быстрого повторения.
д., представлены в простой форме для тщательного изучения. обучения, а также для быстрого повторения.
Глава 1: Синтетические волокна и пластмассы
Первая глава программы химии для 8 класса – Синтетические волокна и пластмассы. Эта глава посвящена одежде, которую мы носим каждый день и которая состоит из тканей. Кроме того, синтетические волокна и пластмассы похожи на натуральные волокна, состоящие из очень крупных единиц. Здесь, в этой главе, мы рассмотрели от основного введения в синтетические волокна до их различных типов и многое другое о пластмассах. Ниже приведен список статей, которые содержат помощь для получения более подробной информации о синтетических волокнах и пластмассах:
- Синтетические и натуральные волокна
- Типы синтетических волокон
- Полиэтилентерефталат
- Характеристики синтетических волокон
- Что такое пластик?
- Биоразлагаемые и небиоразлагаемые материалы
- Загрязнение пластиком
Глава 2: Металлы и неметаллы
Металлы и неметаллы — это вторая глава в учебной программе 8 класса по химии. Эта глава дает нам знания об окружающих нас вещах, которые подразделяются на металлы и неметаллы. Металлы — это материалы, которые являются хорошими проводниками тепла и электричества, такие как железо и т. д. Однако неметаллы — это материалы, которые плохо проводят тепло и электричество, такие как углерод и т. д. Ниже приведены ссылки на статьи, которые охватывают все основная информация о материалах: металлы и неметаллы:
Эта глава дает нам знания об окружающих нас вещах, которые подразделяются на металлы и неметаллы. Металлы — это материалы, которые являются хорошими проводниками тепла и электричества, такие как железо и т. д. Однако неметаллы — это материалы, которые плохо проводят тепло и электричество, такие как углерод и т. д. Ниже приведены ссылки на статьи, которые охватывают все основная информация о материалах: металлы и неметаллы:
- Металлы, неметаллы и металлоиды
- Свойства металлов, неметаллов и металлоидов
- Физические свойства металлов и неметаллов
- Химические свойства металлов и неметаллов
- Ряд металлов
- Применение of Metals and Non-metals
Глава 3: Уголь и нефть
Глава 3 — одна из самых информативных глав в учебной программе по химии для 8 класса. Как и в этой главе, мы узнаем об энергии и ресурсах. Ископаемое топливо и уголь. Уголь и нефть являются исчерпаемыми или невозобновляемыми ресурсами. Ресурсы присутствуют в природе в ограниченном количестве. В следующем списке статей обсуждаются все основные концепции, а также более глубокое объяснение каждой темы с обсуждением некоторых решенных примеров вопросов для быстрого понимания:
В следующем списке статей обсуждаются все основные концепции, а также более глубокое объяснение каждой темы с обсуждением некоторых решенных примеров вопросов для быстрого понимания:
- Исчерпаемые и неисчерпаемые природные ресурсы
- Что такое ископаемое топливо?
- Продукты угля: кокс, каменноугольная смола и каменноугольный газ
- Что такое нефть? – Возникновение, очистка, образование, использование
- Нефтепродукты
- Фракционная перегонка нефти
- Источники энергии – природный газ, нефтехимия и альтернативные источники
Глава 4: четвертое горение и пламя
Химия в программе естественных наук 8 класса. В этой главе обсуждается важнейший химический процесс, называемый горением, при котором вещество вступает в реакцию с кислородом с выделением тепла и света. Например, когда горит спичка, она воспламеняется пламенем и, таким образом, также дает тепло. Пламя – это газообразная и видимая часть огня. Теперь давайте обсудим темы, связанные с горением и пламенем, в следующих статьях:
- Горючие и негорючие вещества
- Какие условия необходимы для горения?
- Как работают безопасные спички?
- Типы горения
- Горение топлива – определение, типы, структура пламени
Глава 5: Загрязнение воздуха и воды
Глава 5 в классе 8 химии – это загрязнение воздуха и воды.


 ).
). Для этого находите тему, прошедшую на уроке и
последовательно переходите по ссылкам на информационные ресурсы, которые
окажут Вам неоценимую помощь в подготовке домашнего материала. Желаю
успешного дистанционного обучения и отличных знаний по химии!
Для этого находите тему, прошедшую на уроке и
последовательно переходите по ссылкам на информационные ресурсы, которые
окажут Вам неоценимую помощь в подготовке домашнего материала. Желаю
успешного дистанционного обучения и отличных знаний по химии!

 1-2 стр.47
1-2 стр.47