ГДЗ Алгебра Зив 7 класс Дидактические
Подробные решения по алгебре за 7 класс авторы Зив, Гольдич
Для семиклассников изучение алгебры является чем-то новым и необычным. Перейти от простой математики к умножению и делению алгебраических дробей – занятие не из легких даже для отличников. Что уж тут говорить о школьниках, особо не блещущих знаниями. Именно поэтому учителя настоятельно рекомендуют перед контрольными пользоваться гдз по алгебре дидактические материалы за 7 класс Зив для повторения и изученного на уроках материала. Сложные системы линейных уравнений больше не будут казаться нерешаемыми, стоит лишь уделить время практике. Правильные решения позволят быстро сверить ответы и значительно сэкономить время при подготовке к проверочной работе на уроке.
Кто активно применяет онлайн помощники в учебном процессе?
Среди тех, кто может активно использовать сборник готовых заданий к дидактическим материалам по алгебре за 7 класс авторов Зив, Гольдич стоит отметить:
- отличников, занимающихся самоподготовкой к предстоящим самостоятельным и контрольным работам, а также к олимпиадам.
 Систематическая работа с пособием и планомерное выполнение заданий позволят идти по любой теме с опережением;
Систематическая работа с пособием и планомерное выполнение заданий позволят идти по любой теме с опережением; - семиклассников, не особо разбирающихся в предмете, но желающих подтянуть знания по пройденным темам. Опираясь на приведенные в решебнике примеры, школьник быстро разберется в свойствах арифметических действий с многочленами;
- родителей, желающих помочь своим детям в подготовке к контрольной работе. Даже если мама и папа уже не совсем помнят, как построить график функции в системе координат, или решить задачу с помощью системы уравнений;
- репетиторов, занимающихся с семиклассниками. Для внеклассной работы такие учебно-методические пособия подходят просто идеально. Ведь в них ответы разобраны в соответствии с требованиями Министерства Образования РФ;
- школьников, учащихся удаленно. На дистанционном обучении подготовиться к предстоящим проверочным работам можно лишь имея хорошее подспорье в виде дополнительной учебной литературы.
Неоспоримые плюсы готовых домашних заданий
Для большинства школьников подробные ответы по алгебре 7 класс к дидактическим материалам (авторы Зив, Гольдич) будут настоящим подарком. Ведь пользуясь еуроки ГДЗ можно за пару минут проверить все ответы и разобрать ошибки. Пользу отмечают даже учителя-методисты:
Ведь пользуясь еуроки ГДЗ можно за пару минут проверить все ответы и разобрать ошибки. Пользу отмечают даже учителя-методисты:
- правильность составления ответов, в соответствии с текущей школьной программой;
- доступность с любого устройства, мобильного или стационарного компьютера в любое время суток и из любого места;
- актуальность информации, так как база сайта постоянно обновляется и дополняется;
- практичность размещения информации и удобный поиск. Найти нужный ответ и разобраться в решении можно за считанные минуты;
- полностью бесплатная платформа, позволяющая всем в равных условиях пользоваться дополнительной учебно-практической литературой.
Стоит потратить немного времени, научиться анализировать свою работу и этого будет достаточно, чтобы заметно улучшить оценки. Любой семиклассник будет рад такой возможности, ведь кроме алгебры есть еще много других предметов. Не говоря уже про отдых и увлекательные хобби.
ГДЗ Алгебра Зив 7 класс Дидактические Номер Вариант 7 СР-7.
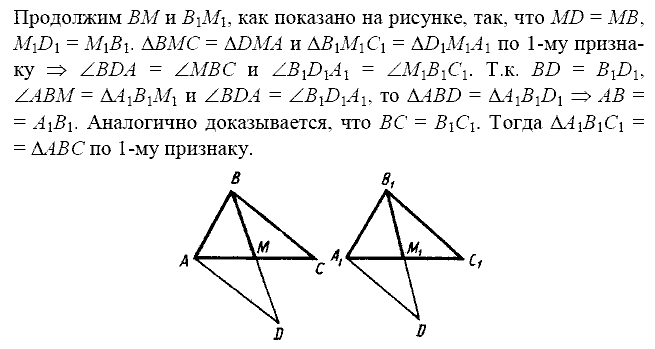 Стандартный вид одночлена. Умножение одночленов
Стандартный вид одночлена. Умножение одночленовСодержание
Авторы:Зив, Гольдич
Изд-во:Петроглиф
Вид УМК:дидактические материалы
Смотреть правильно оформленное решениe и ответ на задание Вариант 7 по алгебре 7 класс дидактические материалы автор(ы) Зив, Гольдич
Скачать решениеСообщи об ошибке или поделись идеей💡
Мне не нравится на сайте, измените:Сделайте так, чтобы можно было:Решение неправильно/опечатка
Содержание
Вариант 4Вариант 5Вариант 6Вариант 7Вариант 8
Похожие решебники по алгебре 7 класс
Учебник
Учебник
Учебник
Учебник
Учебник
org/Book»>Учебник
КИМ
Контрольные
Контрольные
-
Дидактич.
Контрольные
Тетрадь
Учебник
Дидактич.
Контрольные
Контрольные
Проверочные
Тетрадь
org/Book»>Самостоят.
Тесты
Учебник
Дидактич.
Дидактич.
Дидактич.
Дидактич.
Контрольные
Контрольные
Тетрадь
Тетрадь
Тетрадь
org/Book»>Тесты
-
Тесты
Тесты
Тесты
Тетрадь
Дидактич.
Дидактич.
КИМ
Контрольные
Тетрадь
Тетрадь
Тетрадь
Тетрадь
Контрольные
Тесты
Тесты
Учебник
Самостоят.
Тетрадь
Тесты
Тестирование антитела PD-1, MK3475, вводимого вместе с зив-афлиберцептом у пациентов с запущенным раком — полный текст
| Онкологический центр Моффит-Интернэшнл Плаза | |
| Тампа, Флорида, США, 33607 | |
| Онкологический центр Моффитта — кампус Мак-Кинли | |
| Тампа, Флорида, США, 33612 | |
| Онкологический центр Моффита | |
| Тампа, Флорида, США, 33612 | |
| Клиника развивающей терапии Национального института рака | |
| Бетесда, Мэриленд, США, 20892 | |
| Клинический центр Национального института здравоохранения | |
| Бетесда, Мэриленд, США, 20892 | |
| Brigham and Women’s Hospital | |
| Бостон, Массачусетс, США, 02115 | |
| Онкологический институт Дана-Фарбер | |
| Бостон, Массачусетс, США, 02215 | |
| BCCA-Ванкуверский онкологический центр | |
| Ванкувер, Британская Колумбия, Канада, V5Z 4E6 | |
| Университетская сеть здравоохранения – Больница принцессы Маргарет | |
| Торонто, Онтарио, Канада, M5G 2M9 | |
| Главный исследователь: | Фрэнк С Ходи | Дана-Фарбер — Гарвардский онкологический центр LAO |
FDA США одобрило ZALTRAP® (зив-афлиберцепт) после приоритетной проверки ранее леченного метастатического колоректального рака
ПАРИЖ и ТЭРРИТАУН, штат Нью-Йорк, 3 августа 2012 г. SNY) и Regeneron Pharmaceuticals, Inc. (NASDAQ: REGN ) сегодня объявили, что Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило ZALTRAP 9.0132 ® (зив-афлиберцепт) Инъекция для внутривенной инфузии в комбинации с 5-фторурацилом, лейковорином, иринотеканом (FOLFIRI) для пациентов с метастатическим колоректальным раком (мКРР), резистентным или прогрессирующим после схемы, содержащей оксалиплатин.
SNY) и Regeneron Pharmaceuticals, Inc. (NASDAQ: REGN ) сегодня объявили, что Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило ZALTRAP 9.0132 ® (зив-афлиберцепт) Инъекция для внутривенной инфузии в комбинации с 5-фторурацилом, лейковорином, иринотеканом (FOLFIRI) для пациентов с метастатическим колоректальным раком (мКРР), резистентным или прогрессирующим после схемы, содержащей оксалиплатин.
Чтобы просмотреть мультимедийные ресурсы, нажмите: http://www.multivu.com/mnr/57253-sanofi-fda-approves-zaltrap-ziv-aflibercept
«Существуют ограниченные возможности лечения пациентов с метастатическим колоректальным раком которые устойчивы или чье заболевание прогрессировало после схемы, содержащей оксалиплатин»
 «Одобрение ZALTRAP в сочетании со схемой химиотерапии FOLFIRI предлагает еще один вариант лечения и является долгожданной новостью для пациентов с метастатическим колоректальным раком и их врачей».
«Одобрение ZALTRAP в сочетании со схемой химиотерапии FOLFIRI предлагает еще один вариант лечения и является долгожданной новостью для пациентов с метастатическим колоректальным раком и их врачей». ZALTRAP был одобрен после приоритетной проверки FDA. Приоритетный обзор — это обозначение методов лечения, которые предлагают значительные достижения в лечении или обеспечивают лечение там, где не существует адекватной терапии. Заявки на регистрацию ZALTRAP также находятся на рассмотрении Европейского агентства по лекарственным средствам (EMA) и других регулирующих органов по всему миру.
«Колоректальный рак является одним из самых смертоносных видов рака и является причиной более полумиллиона смертей во всем мире каждый год», — сказал , доктор медицинских наук, старший вице-президент и глава Sanofi Oncology. «Санофи надеется сделать ZALTRAP как можно скорее доступным для пациентов с метастатическим колоректальным раком, ранее получавших лечение по схеме, содержащей оксалиплатин».
Одобрение ZALTRAP было основано на данных базового исследования III фазы VELOR, многонационального рандомизированного двойного слепого исследования, в котором FOLFIRI сравнивали в комбинации с ZALTRAP или плацебо при лечении пациентов с мКРР. В исследование были рандомизированы 1226 пациентов с мКРР, которые ранее получали лечение по схеме, содержащей оксалиплатин. Двадцать восемь процентов пациентов в исследовании ранее получали терапию бевацизумабом. Первичной конечной точкой была общая выживаемость. Вторичные конечные точки включали выживаемость без прогрессирования, общую частоту ответа и безопасность.
«Одобрение нового ингибитора ангиогенеза ZALTRAP предоставляет новую возможность для удовлетворения неудовлетворенных медицинских потребностей в этой популяции пациентов», — сказал Джордж Д. Янкопулос, доктор медицинских наук, главный научный сотрудник Regeneron и президент Исследовательские лаборатории Регенерона. «Однако по-прежнему существует потребность в разработке новых методов лечения рака. Regeneron и Sanofi продолжают выделять ресурсы на поиск новых экспериментальных методов лечения и комбинаций».
Regeneron и Sanofi продолжают выделять ресурсы на поиск новых экспериментальных методов лечения и комбинаций».
Результаты исследования VELOR
Исследование VELOR показало, что у пациентов, ранее получавших лечение по схеме, содержащей оксалиплатин, добавление ZALTRAP к FOLFIRI значительно улучшило медиану выживаемости с 12,06 до 13,50 месяцев (HR=0,817 (95% ДИ от 0,714 до 0,935; p= 0,0032), относительное снижение риска на 18. Также наблюдалось значительное улучшение выживаемости без прогрессирования заболевания с 4,67 до 6,90 месяцев (HR=0,758 95% ДИ от 0,661 до 0,869; p=0,00007), снижение относительного риска на 24%. Общая частота ответов в группе ZALTRAP плюс FOLFIRI составила 19.0,8% против 11,1% для FOLFIRI (p=0,0001).
Наиболее частыми побочными реакциями (все степени, частота ≥20%), о которых сообщалось при более высокой частоте (разница между группами 2% или более) в группе ZALTRAP/FOLFIRI, в порядке убывания частоты, были лейкопения, диарея, нейтропения. , протеинурия, повышение уровня АСТ, стоматит, утомляемость, тромбоцитопения, повышение уровня АЛТ, артериальная гипертензия, снижение массы тела, снижение аппетита, носовое кровотечение, боль в животе, дисфония, повышение уровня креатинина в сыворотке крови и головная боль. Наиболее частыми побочными реакциями 3-4 степени (≥5%), о которых сообщалось при более высокой частоте (2% или больше разницы между группами) в группе ZALTRAP/FOLFIRI, в порядке убывания частоты были нейтропения, диарея, гипертония, лейкопения. , стоматит, утомляемость, протеинурия и астения.
, протеинурия, повышение уровня АСТ, стоматит, утомляемость, тромбоцитопения, повышение уровня АЛТ, артериальная гипертензия, снижение массы тела, снижение аппетита, носовое кровотечение, боль в животе, дисфония, повышение уровня креатинина в сыворотке крови и головная боль. Наиболее частыми побочными реакциями 3-4 степени (≥5%), о которых сообщалось при более высокой частоте (2% или больше разницы между группами) в группе ZALTRAP/FOLFIRI, в порядке убывания частоты были нейтропения, диарея, гипертония, лейкопения. , стоматит, утомляемость, протеинурия и астения.
О препарате ZALTRAP ® (зив-афлиберцепт) для инъекций для внутривенных инфузий
ZALTRAP представляет собой рекомбинантный слитый белок, который действует как растворимый рецептор, который связывается с фактором роста эндотелия сосудов-А (VEGF-A), VEGF-B и плацентарный фактор роста (PIGF). Подавление этих факторов может привести к снижению неоваскуляризации и снижению проницаемости сосудов. Санофи планирует сделать ZALTRAP доступным в США в третьем квартале 2012 года. В соответствии с условиями соглашения о сотрудничестве Sanofi и Regeneron поровну делят глобальную прибыль ZALTRAP после того, как Regeneron возьмет на себя обязательство погасить свою долю расходов на разработку. В США ZALTRAP является зарегистрированным товарным знаком Regeneron Pharmaceuticals, Inc.
В соответствии с условиями соглашения о сотрудничестве Sanofi и Regeneron поровну делят глобальную прибыль ZALTRAP после того, как Regeneron возьмет на себя обязательство погасить свою долю расходов на разработку. В США ZALTRAP является зарегистрированным товарным знаком Regeneron Pharmaceuticals, Inc.
Важная информация о безопасности для Zaltrap ®
ПРЕДУПРЕЖДЕНИЕ: кровоизлияние, желудочно -кишечная перфорация, скомпрометированное заживление раны
Searre, и иногда фатальные, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы, которые были зарегистрированы. получил ZALTRAP в сочетании с FOLFIRI. Мониторинг пациентов для признаков и симптомов кровотечения GI и других тяжелых кровотечений. Не назначайте ZALTRAP пациентам с сильным кровотечением.
получил ZALTRAP в сочетании с FOLFIRI. Мониторинг пациентов для признаков и симптомов кровотечения GI и других тяжелых кровотечений. Не назначайте ZALTRAP пациентам с сильным кровотечением.
Перфорация желудочно-кишечного тракта, включая перфорацию ЖКТ со смертельным исходом, может возникнуть у пациентов, получающих ZALTRAP. Прекратите терапию ZALTRAP у пациентов с перфорацией желудочно-кишечного тракта.
У пациентов, получающих ZALTRAP/FOLFIRI, может наблюдаться тяжелое нарушение заживления ран. Прекратите применение ZALTRAP у пациентов с нарушением заживления ран. Приостановите прием ZALTRAP не менее чем за 4 недели до плановой операции и не возобновляйте прием ZALTRAP как минимум в течение 4 недель после серьезной операции и до полного заживления хирургической раны.
ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ
- Пациенты, получающие ZALTRAP, имеют повышенный риск кровотечений, включая тяжелые и иногда фатальные геморрагические явления.

- Мониторинг пациентов на наличие признаков и симптомов кровотечения.
- Не назначайте ZALTRAP пациентам с сильным кровотечением.
- Прекратите применение ZALTRAP у пациентов с тяжелым кровотечением.
90–200 Перфорация желудочно-кишечного тракта, включая перфорацию желудочно-кишечного тракта со смертельным исходом, может возникнуть у пациентов, получающих ZALTRAP. - Мониторинг пациентов на наличие признаков и симптомов перфорации желудочно-кишечного тракта.
- Прекратите применение ZALTRAP у пациентов с перфорацией желудочно-кишечного тракта.
- Прекратите применение ZALTRAP у пациентов с нарушением заживления ран.
- Приостановить ZALTRAP как минимум на 4 недели до плановой операции
- Не начинайте/возобновляйте ZALTRAP, по крайней мере, через 4 недели после операции и полного заживления хирургической раны.
- Образование свищей с поражением желудочно-кишечного тракта и других органов чаще встречается у пациентов, получающих ZALTRAP.
 Прекратите терапию ZALTRAP у пациентов, у которых развилась фистула.
Прекратите терапию ZALTRAP у пациентов, у которых развилась фистула. - У пациентов, получающих ZALTRAP, наблюдался повышенный риск артериальной гипертензии 3-4 степени.
- Контролируйте артериальное давление каждые две недели или чаще и назначайте соответствующую антигипертензивную терапию во время лечения ZALTRAP.
- Временно приостановить прием ZALTRAP до достижения контроля над артериальной гипертензией и снизить дозу ZALTRAP до 2 мг/кг для последующих циклов.
- Прекратите применение ZALTRAP у пациентов с гипертоническим кризом.
- Артериальные тромбоэмболические осложнения (АТЭ), включая транзиторную ишемическую атаку, нарушение мозгового кровообращения и стенокардию, чаще возникали у пациентов, получавших ЗАЛТРАП. Прекратите применение ZALTRAP у пациентов с ATE.
- Тяжелая протеинурия, нефротический синдром и тромботическая микроангиопатия (ТМА) чаще возникали у пациентов, получавших ZALTRAP.
- Приостановить прием Залтрапа при протеинурии ≥2 г/24 часа и возобновить прием Залтрапа при протеинурии <2 г/24 часа.

- В случае рецидива приостановить введение до уровня протеинурии <2 г/24 часа, а затем снизить дозу ZALTRAP до 2 мг/кг.
- Прекратите применение ZALTRAP при развитии нефротического синдрома или ТМА.
- Приостановить прием Залтрапа при протеинурии ≥2 г/24 часа и возобновить прием Залтрапа при протеинурии <2 г/24 часа.
- У пациентов, получавших ЗАЛТРАП, наблюдалась более высокая частота нейтропенических осложнений (фебрильная нейтропения и нейтропеническая инфекция).
- Отложить введение ZALTRAP/FOLFIRI до тех пор, пока число нейтрофилов не станет ≥1,5 x 10 9 /л.
- Частота случаев тяжелой диареи и обезвоживания увеличивается у пациентов, получающих ZALTRAP/FOLFIRI.
- Заболеваемость диареей увеличивается у пациентов в возрасте ≥65 лет. Внимательно следите.
- Прекратите применение ZALTRAP у пациентов, у которых развился обратимый синдром задней лейкоэнцефалопатии.
ПОБОЧНЫЕ РЕАКЦИИ
- Наиболее частыми побочными реакциями (все степени, частота ≥20%), о которых сообщалось при более высокой частоте (разница между группами 2% или более) в группе ZALTRAP/FOLFIRI, в порядке убывания частоты, были лейкопения, диарея , нейтропения, протеинурия, повышение уровня АСТ, стоматит, утомляемость, тромбоцитопения, повышение уровня АЛТ, артериальная гипертензия, снижение массы тела, снижение аппетита, носовое кровотечение, боль в животе, дисфония, повышение уровня креатинина в сыворотке крови и головная боль.

- Наиболее частыми побочными реакциями 3–4 степени (≥5%), о которых сообщалось с большей частотой (разница между группами 2% и выше) в группе ZALTRAP/FOLFIRI, в порядке убывания частоты, были нейтропения, диарея, гипертензия, лейкопения, стоматит, утомляемость, протеинурия и астения.
- Инфекции возникали с большей частотой у пациентов, получавших ZALTRAP/FOLFIRI (46%, все степени; 12%, степень 3-4), чем у пациентов, получавших плацебо/FOLFIRI (33%, все степени, 7%, степень 3-4). , включая инфекцию мочевыводящих путей, назофарингит, инфекцию верхних дыхательных путей, пневмонию, инфекцию в месте установки катетера и инфекцию зубов.
- У пациентов с мКРР венозные тромбоэмболические осложнения (ВТЭ), состоящие в основном из тромбоза глубоких вен и легочной эмболии, произошли в 9% пациентов, получавших ZALTRAP/FOLFIRI, и 7% пациентов, получавших плацебо/FOLFIRI.
Щелкните здесь для получения полной информации о назначении ZALTRAP (зив-афлиберцепт) для внутривенных инъекций, включая ПРЕДУПРЕЖДЕНИЕ в штучной упаковке, и посетите: www.![]() ZALTRAP.com
ZALTRAP.com
О колоректальном раке
По оценкам, в 2012 году будет диагностировано более 143 000 новых случаев колоректального рака, и более 51 000 человек умрут от него. Приблизительно 60 процентов случаев колоректального рака диагностируются на местно-распространенной или метастатической стадии. Хотя выживаемость на ранней стадии заболевания относительно высока, после метастазирования колоректального рака в отдаленные органы пятилетняя выживаемость оценивается в 12 процентов.
Во всем мире колоректальный рак является третьим наиболее часто диагностируемым видом рака у мужчин и вторым среди женщин: в 2008 г. было диагностировано более 1,2 миллиона новых случаев. Колоректальный рак, один из самых смертоносных видов рака, стал причиной более 600 000 смертей во всем мире в только 2008 год.
О компании Sanofi Oncology
Базирующаяся в Кембридже, штат Массачусетс, США, и Витри, Франция, компания Sanofi Oncology занимается преобразованием научных данных в эффективные терапевтические средства, которые удовлетворяют неудовлетворенные медицинские потребности больных раком и пациентов с трансплантированными органами. Начиная с глубокого понимания болезни и пациента, Санофи Онкология применяет инновационные подходы к поиску лекарств и клинической разработке с конечной целью предоставить нужные лекарства нужным пациентам, чтобы помочь им жить более здоровой и долгой жизнью. Мы верим в ценность партнерских отношений, которые объединяют наш внутренний научный опыт с опытом отраслевых и академических экспертов. Наш портфель включает 10 продаваемых продуктов и более 15 исследуемых соединений, находящихся в клинической разработке, включая малые молекулы и биологические агенты.
Начиная с глубокого понимания болезни и пациента, Санофи Онкология применяет инновационные подходы к поиску лекарств и клинической разработке с конечной целью предоставить нужные лекарства нужным пациентам, чтобы помочь им жить более здоровой и долгой жизнью. Мы верим в ценность партнерских отношений, которые объединяют наш внутренний научный опыт с опытом отраслевых и академических экспертов. Наш портфель включает 10 продаваемых продуктов и более 15 исследуемых соединений, находящихся в клинической разработке, включая малые молекулы и биологические агенты.
О Санофи
Санофи, глобальный и диверсифицированный лидер в области здравоохранения, открывает, разрабатывает и распространяет терапевтические решения, ориентированные на потребности пациентов. Санофи имеет сильные стороны в области здравоохранения с семью платформами роста: решения для диабета, вакцины для человека, инновационные лекарства, потребительское здравоохранение, развивающиеся рынки, здоровье животных и новый Genzyme. Санофи зарегистрирована в Париже (EURONEXT: SAN) и в Нью-Йорке (NYSE: SNY).
Санофи зарегистрирована в Париже (EURONEXT: SAN) и в Нью-Йорке (NYSE: SNY).
О компании Regeneron Pharmaceuticals, Inc.
Regeneron — полностью интегрированная биофармацевтическая компания, которая занимается поиском, изобретением, разработкой, производством и коммерциализацией лекарств для лечения серьезных заболеваний. Регенерон продает в США три продукта: EYLEA ® (афлиберцепт) для инъекций, ZALTRAP ® (зив-афлиберцепт) для инъекций для внутривенных вливаний и ARCALYST ® (рилонацепт) для инъекций для подкожного применения. Компания Regeneron подала заявку в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) на второе показание для EYLEA. Исследования фазы 3 продолжаются с EYLEA по двум дополнительным показаниям, а также с препаратами-кандидатами сарилумабом и REGN727. Regeneron ведет активные программы исследований и разработок во многих областях заболеваний, включая офтальмологию, воспаление, рак и гиперхолестеринемию. Дополнительная информация и последние выпуски новостей доступны на веб-сайте Regeneron по адресу www.regeneron.com.
Дополнительная информация и последние выпуски новостей доступны на веб-сайте Regeneron по адресу www.regeneron.com.
Санофи Заявления прогнозного характера
Настоящий пресс-релиз содержит заявления прогнозного характера, как они определены в Законе о реформе судебного разбирательства по частным ценным бумагам от 1995 года с поправками. Прогнозные заявления — это заявления, которые не являются историческими фактами. Эти заявления включают прогнозы и оценки и лежащие в их основе предположения, заявления о планах, целях, намерениях и ожиданиях в отношении будущих финансовых результатов, событий, операций, услуг, разработки продуктов и потенциала, а также заявления о будущих результатах. Прогнозные заявления обычно обозначаются словами «ожидает», «предвидит», «полагает», «намеревается», «оценивает», «планирует» и подобными выражениями. Хотя руководство Санофи считает, что ожидания, отраженные в таких прогнозных заявлениях, являются разумными, инвесторы предупреждены о том, что прогнозная информация и заявления подвержены различным рискам и неопределенностям, многие из которых трудно предсказать и которые, как правило, находятся вне контроля Санофи. которые могут привести к тому, что фактические результаты и события будут существенно отличаться от тех, которые выражены, подразумеваются или прогнозируются в прогнозной информации и заявлениях. Эти риски и неопределенности включают, среди прочего, неопределенности, присущие исследованиям и разработкам, будущим клиническим данным и анализу, включая постмаркетинговые, решения регулирующих органов, таких как FDA или EMA, относительно того, следует ли и когда одобрять какое-либо лекарство, устройство. или биологическая заявка, которая может быть подана для любого такого продукта-кандидата, а также их решения относительно маркировки и других вопросов, которые могут повлиять на доступность или коммерческий потенциал таких продуктов-кандидатов, отсутствие гарантии того, что продукты-кандидаты, если они будут одобрены, будут коммерчески успешными, будущее одобрение и коммерческий успех терапевтических альтернатив, способность Группы извлечь выгоду из возможностей внешнего роста, тенденции обменных курсов и преобладающих процентных ставок, влияние политики сдерживания затрат и ее последующие изменения, среднее количество акций в обращении, а также те обсуждались или идентифицировались в публичных документах с Комиссия по ценным бумагам и биржам США и AMF, подготовленные Санофи, в том числе перечисленные в разделах «Факторы риска» и «Предостережение в отношении прогнозных заявлений» в годовом отчете Санофи по форме 20-F за год, закончившийся 31 декабря 2011 г.
которые могут привести к тому, что фактические результаты и события будут существенно отличаться от тех, которые выражены, подразумеваются или прогнозируются в прогнозной информации и заявлениях. Эти риски и неопределенности включают, среди прочего, неопределенности, присущие исследованиям и разработкам, будущим клиническим данным и анализу, включая постмаркетинговые, решения регулирующих органов, таких как FDA или EMA, относительно того, следует ли и когда одобрять какое-либо лекарство, устройство. или биологическая заявка, которая может быть подана для любого такого продукта-кандидата, а также их решения относительно маркировки и других вопросов, которые могут повлиять на доступность или коммерческий потенциал таких продуктов-кандидатов, отсутствие гарантии того, что продукты-кандидаты, если они будут одобрены, будут коммерчески успешными, будущее одобрение и коммерческий успех терапевтических альтернатив, способность Группы извлечь выгоду из возможностей внешнего роста, тенденции обменных курсов и преобладающих процентных ставок, влияние политики сдерживания затрат и ее последующие изменения, среднее количество акций в обращении, а также те обсуждались или идентифицировались в публичных документах с Комиссия по ценным бумагам и биржам США и AMF, подготовленные Санофи, в том числе перечисленные в разделах «Факторы риска» и «Предостережение в отношении прогнозных заявлений» в годовом отчете Санофи по форме 20-F за год, закончившийся 31 декабря 2011 г. За исключением случаев, предусмотренных применимыми закона, Санофи не берет на себя никаких обязательств по обновлению или пересмотру какой-либо прогнозной информации или заявлений.
За исключением случаев, предусмотренных применимыми закона, Санофи не берет на себя никаких обязательств по обновлению или пересмотру какой-либо прогнозной информации или заявлений.
Regeneron Прогнозные заявления
Этот пресс-релиз включает прогнозные заявления, которые связаны с рисками и неопределенностями, связанными с будущими событиями и будущей деятельностью Regeneron, и фактические события или результаты могут существенно отличаться от этих прогнозных. смотря заявления. Эти заявления касаются, и эти риски и неопределенности включают, помимо прочего, характер, сроки и возможный успех и терапевтическое применение продуктов Regeneron, потенциальных продуктов и исследовательских и клинических программ, которые в настоящее время проводятся или планируются, включая ZALTRAP 9, но не ограничиваясь этим.0138 ® (зив-афлиберцепт) , непредвиденные проблемы безопасности, возникающие в результате применения продуктов и кандидатов в продукты у пациентов, вероятность и сроки возможного одобрения регулирующими органами и коммерческого запуска продуктов-кандидатов Regeneron на поздних стадиях, решения регулирующих и административных государственных органов. которые могут задержать или ограничить способность Regeneron продолжать разработку или коммерциализацию продуктов Regeneron и кандидатов в лекарства, конкурирующих препаратов, которые могут превосходить продукты Regeneron и препараты-кандидаты, неопределенность в отношении принятия рынком продукта Regeneron и кандидатов в лекарства, непредвиденные расходы, затраты на разработку , производство и продажа продуктов, возможность отмены или расторжения любого лицензионного соглашения или соглашения о сотрудничестве, включая соглашения Regeneron с Sanofi Group и Bayer HealthCare, без какого-либо успеха продукта, а также риски, связанные с интеллектуальной собственностью третьих лиц, а также предстоящие или будущие судебные разбирательства. отн. есть к этому. Более полное описание этих и других существенных рисков можно найти в документах Regeneron, поданных в Комиссию по ценным бумагам и биржам США, включая форму 10-K за год, закончившийся 31 декабря 2011 г., и форму 10-Q за квартал, закончившийся в июне.
которые могут задержать или ограничить способность Regeneron продолжать разработку или коммерциализацию продуктов Regeneron и кандидатов в лекарства, конкурирующих препаратов, которые могут превосходить продукты Regeneron и препараты-кандидаты, неопределенность в отношении принятия рынком продукта Regeneron и кандидатов в лекарства, непредвиденные расходы, затраты на разработку , производство и продажа продуктов, возможность отмены или расторжения любого лицензионного соглашения или соглашения о сотрудничестве, включая соглашения Regeneron с Sanofi Group и Bayer HealthCare, без какого-либо успеха продукта, а также риски, связанные с интеллектуальной собственностью третьих лиц, а также предстоящие или будущие судебные разбирательства. отн. есть к этому. Более полное описание этих и других существенных рисков можно найти в документах Regeneron, поданных в Комиссию по ценным бумагам и биржам США, включая форму 10-K за год, закончившийся 31 декабря 2011 г., и форму 10-Q за квартал, закончившийся в июне. 30, 2012. Regeneron не берет на себя никаких обязательств по публичному обновлению любых прогнозных заявлений, будь то в результате получения новой информации, будущих событий или иным образом, если это не требуется по закону.
30, 2012. Regeneron не берет на себя никаких обязательств по публичному обновлению любых прогнозных заявлений, будь то в результате получения новой информации, будущих событий или иным образом, если это не требуется по закону.
Контакты: | |
| | |
Санофи: | Регенерон: |
Лорен Мусто | Маниша Нарасимхан |
Global Oncology Division Communications | Связи с инвесторами |
Тел.: 1 (617) 768-1993; Мобильный 1 (781) 572-1147 | Тел.: 1 (914) 847-5126 |
Электронная почта: [email protected] | Электронная почта: [email protected] |
| | |
Кэрри Браун | Питер Дворкин |
Связь с отделом онкологии США | Связи со СМИ |
Тел: 1 (908) 981-6486; Мобильный 1 (908) 247-6006 | Тел. |


 Систематическая работа с пособием и планомерное выполнение заданий позволят идти по любой теме с опережением;
Систематическая работа с пособием и планомерное выполнение заданий позволят идти по любой теме с опережением;
 Прекратите терапию ZALTRAP у пациентов, у которых развилась фистула.
Прекратите терапию ZALTRAP у пациентов, у которых развилась фистула.

